Прэмія Ласкера за фундаментальныя медыцынскія даследаванні ў гэтым годзе была прысуджана Дэмісу Хасабісу і Джону Джамперу за іх унёсак у стварэнне сістэмы штучнага інтэлекту AlphaFold, якая прадказвае трохмерную структуру бялкоў на аснове паслядоўнасці амінакіслот першага парадку.
Іх вынікі вырашаюць праблему, якая даўно турбуе навуковую супольнасць, і адкрываюць дзверы для паскарэння даследаванняў у біямедыцынскай галіне. Бялкі адыгрываюць ключавую ролю ў развіцці захворванняў: пры хваробе Альцгеймера яны згортваюцца і зліпаюцца; пры раку іх рэгуляторная функцыя губляецца; пры прыроджаных парушэннях абмену рэчываў яны парушаюцца; пры мукавісцыдозе яны трапляюць у няправільнае месца ў клетцы. Гэта толькі некаторыя з шматлікіх механізмаў, якія выклікаюць захворванні. Падрабязныя мадэлі структуры бялкоў могуць забяспечыць атамныя канфігурацыі, кіраваць распрацоўкай або адборам малекул з высокай афіннасцю і паскараць адкрыццё лекаў.
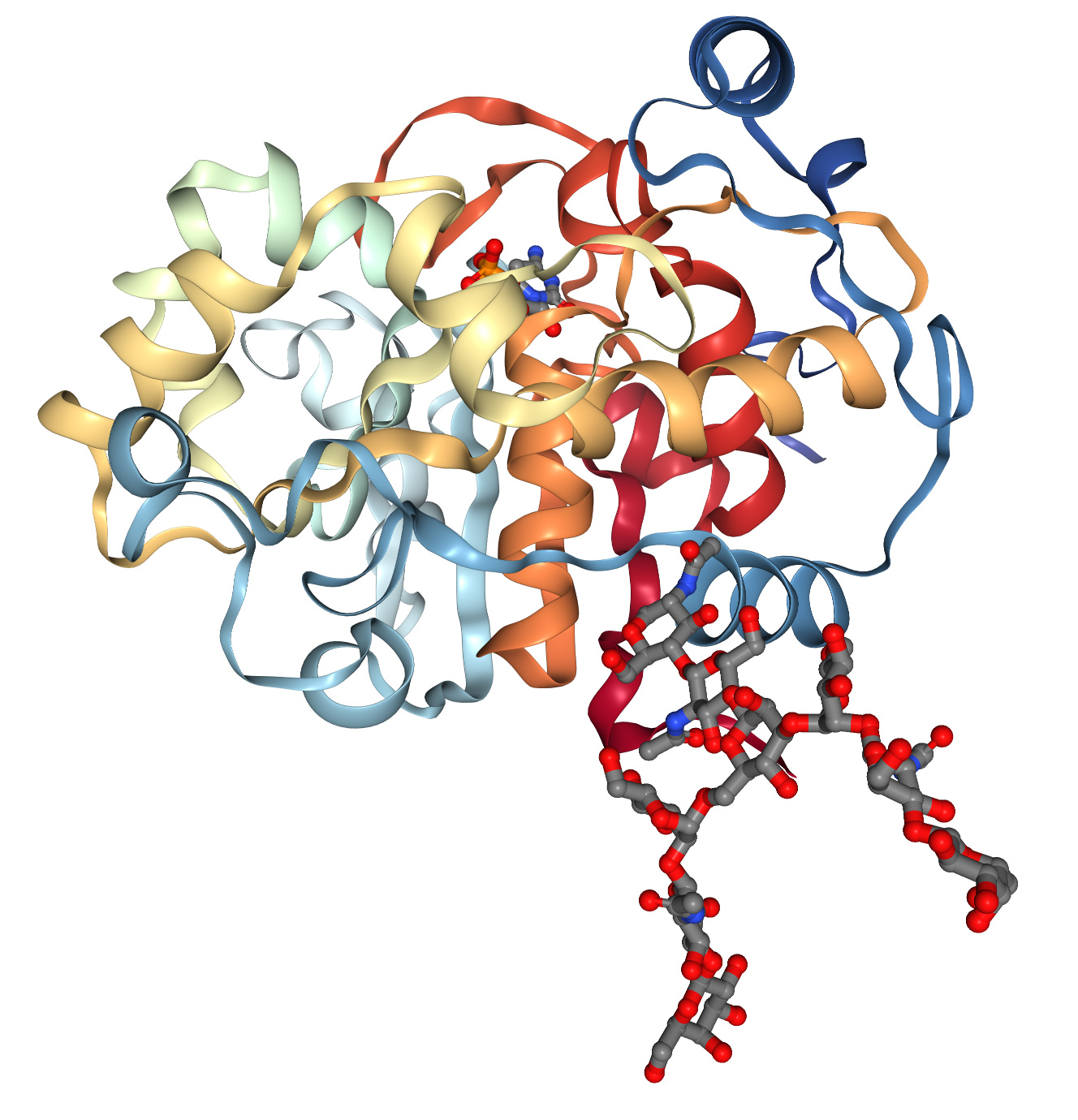
Структуры бялкоў звычайна вызначаюцца з дапамогай рэнтгенаўскай крышталаграфіі, ядзернага магнітнага рэзанансу і крыяэлектроннай мікраскапіі. Гэтыя метады дарагія і працаёмкія. У выніку існуючыя трохмерныя базы дадзеных структуры бялкоў змяшчаюць толькі каля 200 000 структурных дадзеных, у той час як тэхналогія секвенавання ДНК дала больш за 8 мільёнаў паслядоўнасцей бялкоў. У 1960-х гадах Анфінсен і інш. выявілі, што аднамерная паслядоўнасць амінакіслот можа спантанна і паўторна згортвацца ў функцыянальную трохмерную канфармацыю (малюнак 1А), і што малекулярныя «шапероны» могуць паскорыць і палегчыць гэты працэс. Гэтыя назіранні прывялі да 60-гадовай праблемы ў малекулярнай біялогіі: прагназавання трохмернай структуры бялкоў па аднамернай паслядоўнасці амінакіслот. Дзякуючы поспеху праекта «Геном чалавека» наша здольнасць атрымліваць аднамерныя паслядоўнасці амінакіслот значна палепшылася, і гэтая праблема стала яшчэ больш актуальнай.
Прадказаць структуру бялкоў складана па некалькіх прычынах. Па-першае, усе магчымыя трохмерныя пазіцыі кожнага атама ў кожнай амінакіслаце патрабуюць шмат даследаванняў. Па-другое, бялкі максімальна выкарыстоўваюць дапаўняльнасць у сваёй хімічнай структуры для эфектыўнай канфігурацыі атамаў. Паколькі бялкі звычайна маюць сотні «донараў» вадародных сувязей (звычайна кісларод), якія павінны знаходзіцца блізка да «акцэптара» вадародных сувязей (звычайна азот, звязаны з вадародам), можа быць вельмі цяжка знайсці канфармацыі, дзе амаль кожны донар знаходзіцца блізка да акцэптара. Па-трэцяе, існуе абмежаваная колькасць прыкладаў для навучання эксперыментальных метадаў, таму неабходна разумець патэнцыйныя трохмерныя ўзаемадзеянні паміж амінакіслотамі на аснове аднамерных паслядоўнасцей, выкарыстоўваючы інфармацыю аб эвалюцыі адпаведных бялкоў.
Фізіка ўпершыню была выкарыстана для мадэлявання ўзаемадзеяння атамаў у пошуку найлепшай канфармацыі, і быў распрацаваны метад прагназавання структуры бялкоў. Карплус, Левіт і Уоршэль былі ўзнагароджаны Нобелеўскай прэміяй па хіміі ў 2013 годзе за сваю працу па вылічальным мадэляванні бялкоў. Аднак метады, заснаваныя на фізіцы, з'яўляюцца вылічальна дарагімі і патрабуюць прыблізнай апрацоўкі, таму дакладныя трохмерныя структуры немагчыма прадказаць. Іншы падыход, «заснаваны на ведах», заключаецца ў выкарыстанні баз дадзеных вядомых структур і паслядоўнасцей для навучання мадэляў з дапамогай штучнага інтэлекту і машыннага навучання (AI-ML). Хасабіс і Джампер ужываюць элементы як фізікі, так і AI-ML, але інавацыі і скачок у прадукцыйнасці падыходу ў першую чаргу вынікаюць з AI-ML. Два даследчыкі творча аб'ядналі вялікія публічныя базы дадзеных з вылічальнымі рэсурсамі прамысловага ўзроўню, каб стварыць AlphaFold.
Як мы ведаем, што яны «вырашылі» загадку прагназавання структуры? У 1994 годзе быў заснаваны конкурс крытычнай ацэнкі прагназавання структуры (CASP), які праводзіцца кожныя два гады для адсочвання прагрэсу прагназавання структуры. Даследчыкі будуць дзяліцца аднамернай паслядоўнасцю бялку, структуру якога яны нядаўна вырашылі, але вынікі якога яшчэ не апублікаваныя. Прадказальнік прадказвае трохмерную структуру, выкарыстоўваючы гэтую аднамерную паслядоўнасць, а ацэншчык незалежна ацэньвае якасць прагназаваных вынікаў, параўноўваючы іх з трохмернай структурай, прадстаўленай эксперыментатарам (прадастаўленай толькі ацэншчыку). CASP праводзіць сапраўдныя сляпыя агляды і фіксуе перыядычныя скачкі прадукцыйнасці, звязаныя з метадалагічнымі інавацыямі. На 14-й канферэнцыі CASP у 2020 годзе вынікі прагназавання AlphaFold паказалі такі скачок у прадукцыйнасці, што арганізатары абвясцілі, што праблема прагназавання трохмернай структуры была вырашана: дакладнасць большасці прагнозаў была блізкая да дакладнасці эксперыментальных вымярэнняў.
Шырэйшае значэнне заключаецца ў тым, што праца Хасабіса і Джампера пераканаўча дэманструе, як штучны інтэлект з машынным навучаннем (AI-ML) можа трансфармаваць навуку. Даследаванне паказвае, што AI-ML можа будаваць складаныя навуковыя гіпотэзы з некалькіх крыніц дадзеных, што механізмы ўвагі (падобныя да тых, што ў ChatGPT) могуць выяўляць ключавыя залежнасці і карэляцыі ў крыніцах дадзеных, і што AI-ML можа самастойна ацэньваць якасць сваіх вынікаў. AI-ML па сутнасці займаецца навукай.
Час публікацыі: 23 верасня 2023 г.