Змяшаная гіперліпідэмія характарызуецца падвышаным узроўнем у плазме ліпапратэінаў нізкай шчыльнасці (ЛПНП) і ліпапратэінаў, багатых трыгліцерыдамі, што прыводзіць да падвышанай рызыкі атэрасклератычных сардэчна-сасудзістых захворванняў у гэтай папуляцыі пацыентаў.
ANGPTL3 інгібіруе ліпапратэінліпазу і эндасепіазу, а таксама паглынанне печанню ліпапратэінаў, багатых трыгліцерыдамі. Носьбіты інактываванага варыянту ANGPTL3 мелі больш нізкія ўзроўні трыгліцерыдаў, халестэрыну ЛПНП, халестэрыну ліпапратэінаў высокай шчыльнасці (ЛПВП) і халестэрыну, не звязанага з ЛПВП, а таксама меншы рызыка атэрасклератычных сардэчна-сасудзістых захворванняў. Зодасіран - гэта прэпарат на аснове малой інтэрферуючай РНК (РНК-і), які накіраваны на экспрэсію ANGPTL3 у печані.
Змяшаная гіперліпідэмія азначае падвышаны ўзровень халестэрыну ліпапратэінаў нізкай шчыльнасці (ЛПНП) і ліпапратэінаў, багатых трыгліцерыдамі. Ліпапратэіны, багатыя трыгліцерыдамі (у тым ліку хіламікроны, ліпапратэіны вельмі нізкай шчыльнасці (ЛПНП) і рэшткавы халестэрын), адыгрываюць важную ролю ў развіцці атэрасклератычнага захворвання. Эфектыўнага лячэння змяшанай гіперліпідэміі не існуе.
Вядома, што прэпараты Бэйтса зніжаюць узровень трыгліцерыдаў (ТГ), але гэта зніжэнне абмежаванае. У той жа час прэпараты, якія зніжаюць узровень ТГ, у тым ліку прэпараты Бэйтса (напрыклад, эйказапентаенавая воцатная кіслата і г.д.), не аказваюць істотнага ўплыву на рызыку атэрасклератычных захворванняў, выкліканых падвышаным узроўнем рэшткавага халестэрыну. Акрамя таго, папярэднія даследаванні пацыентаў, якія ўжо прымаюць статыны, паказалі, што камбінаваныя прэпараты, якія зніжаюць узровень ТГ, не зніжаюць рызыку сардэчна-сасудзістых падзей. Гэтыя фактары вельмі ўскладняюць лячэнне змешанай гіперліпідэміі.
ANGPTL3 (ангіяпаэтынападобны бялок 3) рэгулюе метабалізм ліпідаў і ліпапратэінаў, у тым ліку ТГ і халестэрыну ліпапратэінаў невысокай шчыльнасці (ЛПВП), шляхам зварачальнага інгібіравання паглынання ліпапратэінаў ліпазы, эндасепіазы і ліпапратэінаў нізкай шчыльнасці (ЛПНП) рэцэптарамі печані. Было выяўлена, што варыянт інактывацыі ANGPTL3 прыводзіць да павышэння актыўнасці ліпапратэінаў ліпазы і эндасепіазы, што, у сваю чаргу, прыводзіць да нізкага ўзроўню ліпапратэінаў у плазме ў большасці выпадкаў. Да іх адносяцца ліпапратэіны, багатыя трыгліцерыдамі (г.зн. хіламікроны, рэшткавы халестэрын, ЛПДНП, ліпапратэіны сярэдняй шчыльнасці [ЛПНС]), ЛПНП, ліпапратэіны высокай шчыльнасці (ЛПВП), ліпапратэін (а) і іх халестэрынавыя кампаненты. Гетэразіготныя людзі, якія з'яўляюцца носьбітамі гэтага варыянту, маюць прыблізна на 40% меншы рызыка атэрасклератычных захворванняў, і ніякага неспрыяльнага клінічнага фенатыпу не выяўлена. ANGPTL3 экспрэсуецца ў печані, і тэрапія глушэння генаў, накіраваная на яго мРНК, вядомая як прэпараты на аснове малых інтэрферуючых РНК (siRNA), з'яўляецца перспектыўным гібрыдным метадам лячэння гіперліпідэміі.
12 верасня 2024 года ў часопісе «New England Journal of Medicine» (NEJM) былі апублікаваныя вынікі даследавання ARCHES 2, якое пацвярджае, што прэпарат з міРНК зодасиран значна зніжае ўзровень трыгліцэрынаў у пацыентаў са змяшанай гіперліпідэміяй [1]. ARCHES-2 — гэта двайное сляпое плацеба-кантраляванае даследаванне фазы 2b з выкарыстаннем розных доз. У даследаванне былі ўключаны 204 пацыенты са змяшанай гіперліпідэміяй (узровень трыгліцэрынаў нашча 150–499 мг/дл, узровень ХС ЛПНП ≥70 мг/дл або ўзровень ХС не-ЛПВП ≥100 мг/дл). Яны былі падзелены на групы зодасирана 50 мг, 100 мг, 200 мг і кантрольную групу плацеба. Пацыенты атрымлівалі падскурныя ін'екцыі на 1-м і 12-м тыднях і атрымлівалі наступную прафілактыку да 36-га тыдня.
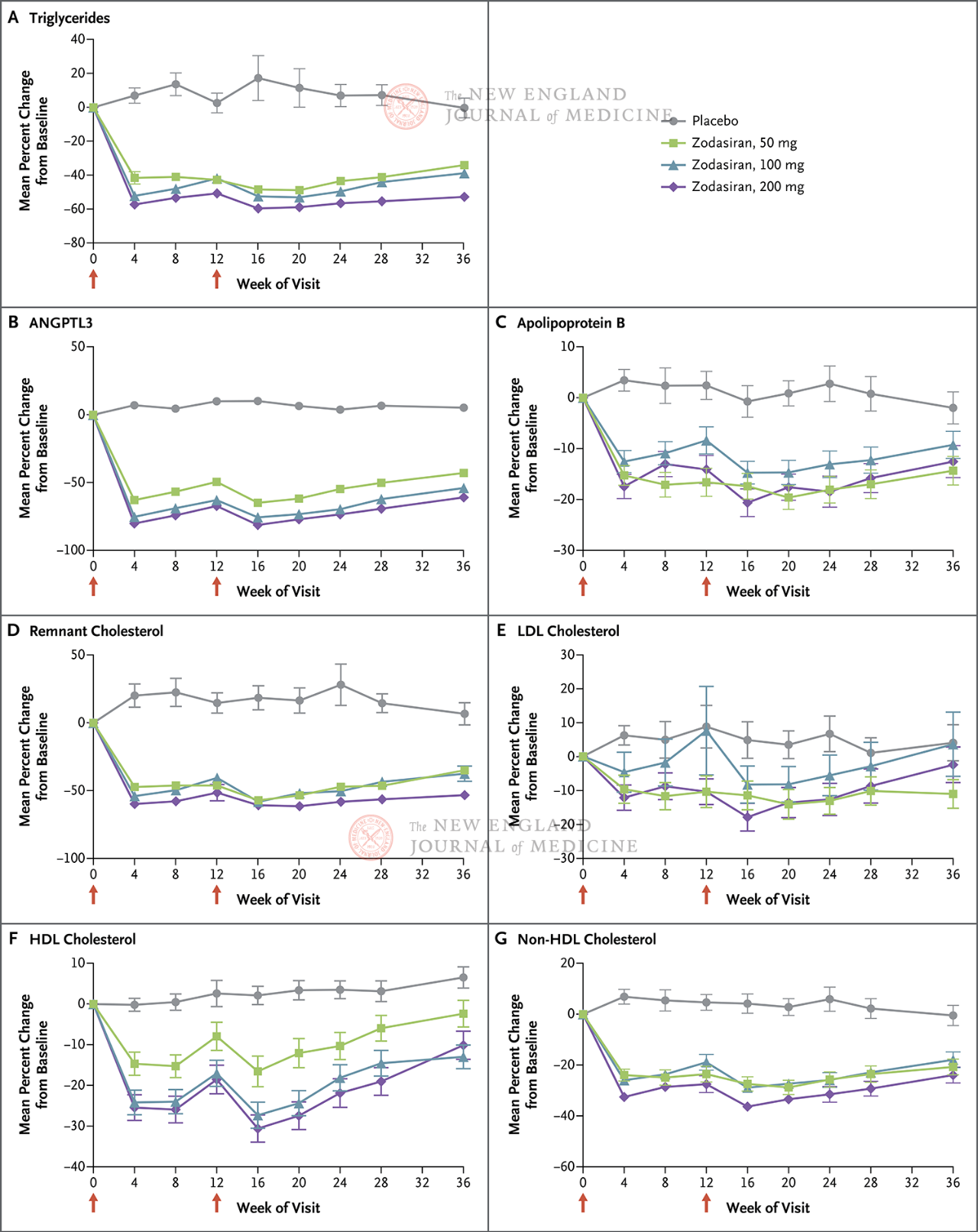
Першаснай канчатковай кропкай было працэнтнае змяненне ўзроўню ТГ ад пачатковага ўзроўню да 24-га тыдня. Даследаванне паказала, што да 24-га тыдня ўзровень ТГ у групе зодасирана значна знізіўся дозазалежным чынам (узровень ТГ у кожнай дозавай групе знізіўся на 51, 57 і 63 працэнтныя пункты адпаведна ў параўнанні з групай плацеба) (P <0,001 для ўсіх параўнанняў). ANGPTL3 таксама знізіўся на 54 працэнтныя пункты, 70 працэнтных пунктаў і 74 працэнтныя пункты адпаведна. Узровень не-ЛПВП знізіўся на 29 працэнтных пунктаў, 29 працэнтных пунктаў і 36 працэнтных пунктаў, узровень апаліпапратэіна B знізіўся на 19 працэнтных пунктаў, 15 працэнтных пунктаў і 22 працэнтныя пункты, а ўзровень ЛПНП знізіўся на 16 працэнтных пунктаў, 14 працэнтных пунктаў і 20 працэнтных пунктаў адпаведна, і гэтыя вынікі захоўваліся да 36-га тыдня. На 24-м тыдні зодасиран...
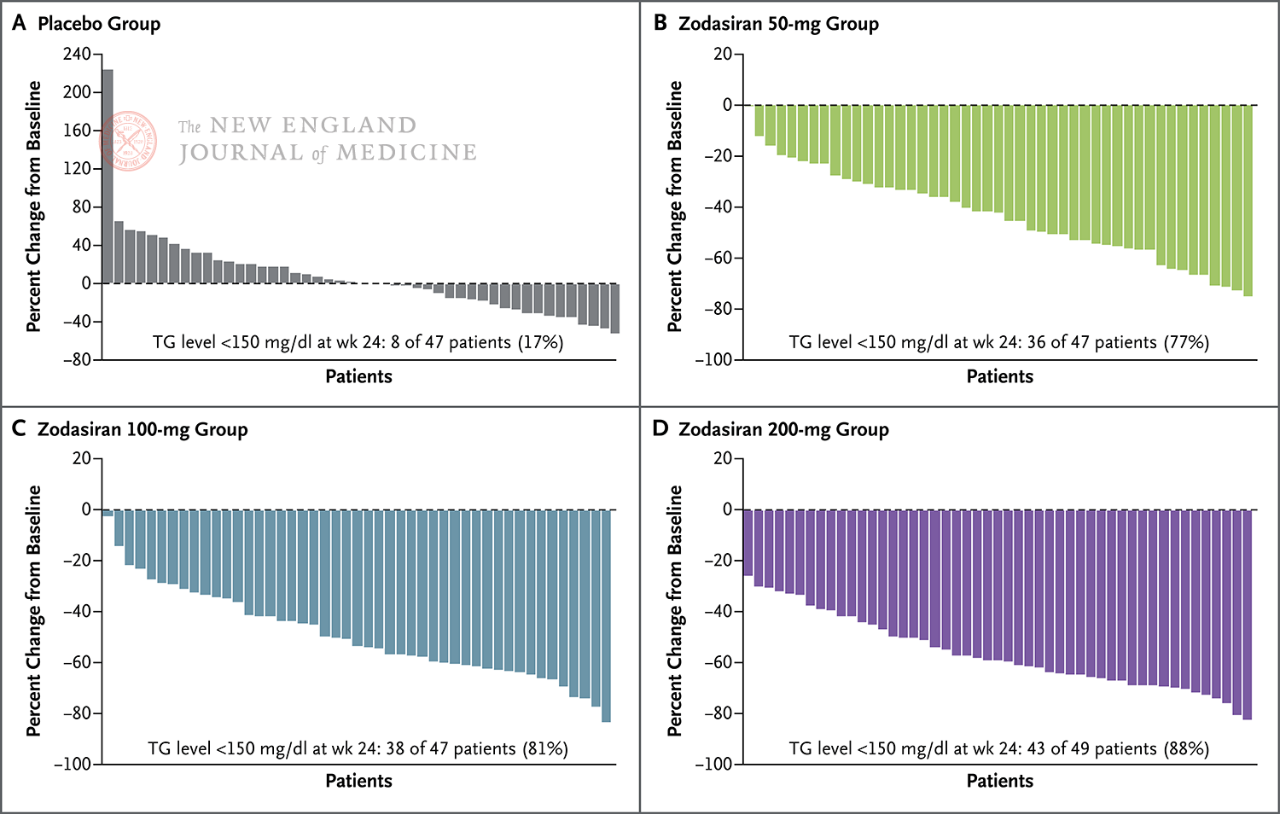
У 88% пацыентаў у групе, якая прымала 200 мг, узровень трыгліцэрыду нашча знізіўся да нормы.
Чырвоныя стрэлкі на 1-ы і 12-ы дні паказваюць прыём зодасирана або плацеба.
Узровень трыгліцэрыдаў нашча знізіўся да нормы на 24-м тыдні (150
мг/дл або менш)
Кожны слуп прадстаўляе аднаго пацыента.
У даследаванні таксама адзначалася, што зотасіран быў бяспечны ва ўсіх дозавых групах, прычым толькі 2 пацыенты спынілі даследаванне з-за пабочных эфектаў (1 у групе плацеба і 1 у групе зотасірана 100 мг). Усе сур'ёзныя пабочныя эфекты ў групе зотасірана аднавіліся да канца даследавання, і ў групе плацеба быў адзін смяротны выпадак. Адзіным пабочным эфектам, які выклікаў заклапочанасць, было павышэнне ўзроўню HBA1c у групе зотасірана 200 мг у параўнанні з плацеба (сярэдняе змяненне ад пачатку да 24-га тыдня [±SD], 0,38±0,66% супраць -0,03±0,88% у пацыентаў з існуючым дыябетам). Пацыенты без дыябету складалі 0,12±0,19% супраць -0,03±0,19%).
У прыватнасці, амаль усе пацыенты ў даследаванні (96%) атрымлівалі статыны (37% з якіх былі статынамі ў высокіх дозах), 1% атрымлівалі інгібітар субтылізіну 9 (PCSK9i), а 21% атрымлівалі фібраты. Такім чынам, даданне зодасирана да існуючага канвенцыйнага рэжыму лячэння ўсё ж дасягнула значнага эфекту зніжэння ўзроўню ліпідаў, што забяспечвае новы рэжым лячэння змешанай гіперліпідэміі ў будучыні.
На 24-м тыдні максімальная доза 200 мг зотасірана ў даследаванні знізіла ўзровень рэшткавага халестэрыну на 34,4 мг/дл у параўнанні з плацеба. Зыходзячы з існуючых мадэляў, чакаецца, што гэта зніжэнне прывядзе да зніжэння асноўных пабочных эфектаў з боку сэрца на 20 працэнтаў. Зодасіран можа выкарыстоўвацца ў якасці монатэрапіі для ўсіх кампанентаў ліпапратэінаў для зніжэння рызыкі сардэчна-сасудзістых падзей у пацыентаў. Таму неабходныя далейшыя даследаванні, каб вызначыць патэнцыял гэтага прэпарата ў зніжэнні рызыкі атэрасклератычных захворванняў.
У фазе 2b, двайным сляпым, рандомізіраваным, плацеба-кантраляваным даследаванні MUIR, апублікаваным адначасова ў NEJM, для лячэння змешанай гіперліпідэміі выкарыстоўваўся іншы прэпарат на аснове міРНК, плозасіран [2]. Плозасіран прызначаны для зніжэння экспрэсіі APOC3, гена, які кадуе апаліпапратэін С3 (APOC3), рэгулятар метабалізму ТГ, у печані, тым самым зніжаючы ўзровень ТГ і рэшткавага халестэрыну. Зніжэнне ўзроўню ТГ і рэшткавага халестэрыну, якое назіралася ў даследаванні, было падобным да таго, што было выяўлена ў даследаванні ARCHES-2. Такім чынам, мяркуецца, што ў пацыентаў са змешанай гіперліпідэміяй абодва прэпараты маюць падобны эфект у зніжэнні ўзроўню ліпапратэінаў, багатых трыгліцерыдамі, і рэшткавага халестэрыну.
Вынікі двух даследаванняў siRNA паказваюць, што гэта вельмі перспектыўны клас прэпаратаў, які адкрые новыя магчымасці для лячэння змешанай гіперліпідэміі і палепшыць сардэчна-сасудзістыя вынікі ў пацыентаў.
Час публікацыі: 15 верасня 2024 г.